|
MỤC TIÊU GIẢNG DẠY
Hiểu
được khái niệm và ý nghĩa của sự dung thứ
Biết được các yếu tố quyết định cảm ứng của dung thứ
Hiểu được cơ chế của cảm ứng dung thứ
Hiểu được các khái niệm về tự miễn dịch và bệnh tật
Biết được các đặc điểm của các bệnh tự miễn dịch chủ
yếu
Biết được các thuyết về nguyên nhân của bệnh tự miễn
|
DUNG THỨ MIỄN DỊCH
GIỚI THIỆU
Dung thứ đề cập đến tính không đáp ứng miễn dịch đặc hiệu
đối với một kháng nguyên đã
từng được tiếp xúc trước đó. Mặc dù hình thức dung thứ quan trọng
nhất là không đáp ứng với các tự kháng nguyên bản thân, nhưng có thể
gây ra sự dung thứ đối với các kháng nguyên không phải của bản thân.
Khi một kháng nguyên gây ra sự dung thứ, nó được gọi là tolerogen.
DUNG THỨ VỚI TỰ KHÁNG NGUYÊN
Chúng ta thường không có đáp ứng miễn dịch mạnh đối với các kháng nguyên
của chính chúng ta (tự kháng nguyên), một hiện tượng gọi là tự dung thứ.
Khi hệ thống miễn dịch nhận ra một tự kháng nguyên và tạo ra một đáp
ứng mạnh mẽ chống lại nó, bệnh tự miễn sẽ phát triển. Tuy nhiên, hệ
thống miễn dịch phải tự nhận MHC để thực hiện đáp ứng chống lại một
kháng nguyên ngoại lai. Do đó, hệ thống miễn dịch liên tục bị thách
thức để phân biệt kháng
nguyên bản thân và không phải
của bản thân và đáp ứng đúng.
CẢM
ỨNG DUNG THỨ VỚI KHÁNG NGUYÊN KHÔNG PHẢI CỦA BẢN THÂN
Sự
dung thứ cũng có thể được tạo ra đối với các kháng nguyên ngoại lai
bằng cách sửa đổi kháng nguyên, bằng cách tiêm kháng nguyên qua các
đường đặc hiệu như uống, đưa kháng nguyên vào khi hệ thống miễn dịch
đang phát triển, v.v ... Một số vi khuẩn và virut đã nghĩ ra những cách
thông minh để gây ra sự dung nạp để vật chủ không giết chết các vi khuẩn
này. Vd: Bệnh nhân mắc bệnh phong không có đáp ứng miễn dịch với
Mycobacterium leprae (Trực khuẩn phong).
DUNG THỨ VỚI CÁC TẾ BÀO VÀ MÔ
Sự
dung thứ đối với các kháng nguyên của tế bào và mô có thể được gây ra
bằng cách tiêm tế bào tạo máu (tế bào gốc) ở trẻ sơ sinh hoặc suy giảm
miễn dịch nghiêm trọng ở động vật (bằng cách chiếu xạ hoặc điều trị
bằng thuốc). Ngoài ra, ghép tủy xương hoặc tuyến ức đồng loài trong
giai đoạn đầu đời dẫn đến khả năng dung thứ các tế bào và mô của người
hiến tặng. Những động vật như vậy được gọi là chimera. Những phát hiện
này là ứng dụng thực tế quan trọng trong ghép tủy xương.
|
| |
DUNG THỨ
VỚI KHÁNG NGUYÊN HÒA TAN
Một trạng
thái dung thứ đối với nhiều loại kháng nguyên phụ thuộc T và không phụ thuộc
T đã đạt được trong các mô hình thí nghiệm khác nhau. Dựa trên những quan sát
này, người ta thấy rằng một số yếu tố quyết định liệu một kháng nguyên sẽ
kích thích đáp ứng miễn dịch hay gây dung thứ (Bảng 1).
|
Bảng
1.
Các yếu tố quyết định gây ra
đáp
ứng
miễn dịch hoặc dung
thứ
sau thử thách với kháng nguyên |
|
Yếu
tố ảnh hưởng đến đáp ứng của kháng nguyên |
Đáp
ứng miễn dịch |
Dung thứ |
|
Hình thái vật lý |
Các phân tử lớn, kết tụ, phức tạp |
Các phân tử hòa tan, không kết tụ, tương đối nhỏ hơn, ít
phức tạp hơn, kháng nguyên không được xử lý bởi APC hoặc được xử lý bởi
tế bào không có MHC lớp II |
|
Đường
vào của kháng nguyên |
Dưới da hoặc tiêm bắp |
Uống hoặc đôi khi tiêm tĩnh mạch |
|
Liều lượng của kháng nguyên |
Liều tối ưu |
Liều lượng rất lớn (hoặc đôi khi rất nhỏ) |
|
Tuổi của động vật đáp ứng |
Già hơn và trưởng thành về mặt miễn dịch |
Sơ sinh (chuột), chưa trưởng thành về mặt miễn dịch |
|
Tình trạng phân chia của tế bào |
Tế bào đã biệt hóa hoàn toàn; tế bào T và B nhớ |
Tương đối không biệt hóa: Tế bào B chỉ có IgM (không có
IgD), tế bào T (ví dụ: tế bào trong vỏ tuyến ức) |
NHỮNG ĐẶC
TRƯNG MIỄN DỊCH CỦA DUNG THỨ
Dung thứ
khác với ức chế miễn dịch không đặc hiệu và suy giảm miễn dịch. Đây là một quá
trình phụ thuộc vào kháng nguyên hoạt hóa để đáp ứng với kháng nguyên. Giống như
đáp ứng miễn dịch, dung thứ là đặc hiệu và giống như bộ nhớ miễn dịch, nó có thể
tồn tại trong tế bào T, tế bào B hoặc cả hai và giống như bộ nhớ miễn dịch, dung
thứ ở mức độ tế bào T kéo dài hơn dung thứ ở mức độ tế bào B.
Việc tạo ra
sự dung thứ các tế bào T dễ dàng hơn và đòi hỏi lượng dung thứ tương đối nhỏ hơn
so với dung thứ của các tế bào B. Duy trì dung thứ miễn dịch đòi hỏi sự bền vững
của kháng nguyên. Sự dung thứ có thể bị phá vỡ một cách tự nhiên (như trong các
bệnh tự miễn) hoặc nhân tạo (như thể hiện ở động vật thí nghiệm, bằng chiếu xạ
tia x, một số phương pháp điều trị bằng thuốc và do tiếp xúc với các kháng
nguyên phản ứng chéo).
Dung thứ có
thể được gây ra cho tất cả các epitop hoặc chỉ một số epitop trên một kháng
nguyên và dung thứ đối với một kháng nguyên duy nhất có thể tồn tại ở mức độ tế
bào B hoặc tế bào T hoặc ở cả hai.
|
| |
CƠ CHẾ CỦA DUNG THỨ
Cơ chế chính xác của cảm ứng và duy trì
dung thứ chưa được hiểu đầy đủ. Tuy nhiên, dữ liệu thí nghiệm chỉ ra một
số khả năng.
Xóa dòng
Các tế bào lympho T và B trong quá trình phát triển
bắt gặp các tự kháng nguyên và các tế bào như vậy trải qua quá trình
xóa dòng thông qua một quá trình được gọi là chết tế bào theo chương
trình. Ví dụ, các tế bào T phát triển trong tuyến ức trước hết biểu
hiện cả CD4 và CD8. Các tế bào đó có cả CD4 và CD8 được gọi là các
tế bào dương tính kép và biểu lộ αβ TCR thấp. Các tế bào như vậy
trải qua chọn lọc dương sau khi tương tác với các phân tử MHC lớp I
hoặc II được biểu lộ trên biểu mô vùng vỏ tuyến ức. Trong quá trình
này, các tế bào có ái tính thấp với MHC được chọn lọc dương. Các tế
bào không được chọn thì chết theo chương trình, một quá trình gọi là
"chết do bỏ rơi". Tiếp theo, các tế bào mất CD4 hoặc CD8. Sau đó,
các tế bào T này gặp phải các peptid tự thân kết hợp với MHC trên
các tế bào có tua. Những tế bào T có thụ thể có ái lực cao đối với
MHC + peptid tự thân trải qua quá trình xóa dòng thì được gọi là lựa
chọn âm tính thông qua chết theo chương trình. Bất kỳ sự xáo trộn
nào trong quá trình này đều có thể dẫn đến việc thoát khỏi các tế
bào T tự phản ứng gây ra bệnh tự miễn. Tương tự như vậy, các tế bào
B non phân chia khi chúng gặp phải tự kháng nguyên là tế bào hay
phân tử hòa tan đều bị xóa dòng. Do đó, việc xóa dòng đóng vai trò
chính trong việc đảm bảo khả năng chống lại tự kháng nguyên.
Dung thứ ngoại vi
Việc xóa dòng không phải là một hệ thống bằng chứng
ngu ngốc và thường các tế bào T và B không thể trải qua quá trình
xóa và do đó các tế bào như vậy có thể gây ra bệnh tự miễn khi chúng
đến các cơ quan lympho ngoại vi. Do đó, hệ thống miễn dịch đã nghĩ
ra một số điểm kiểm tra bổ sung để có thể duy trì khả năng dung thứ.
Chết tế bào bởi sự hoạt hóa
Các tế bào T khi hoạt hóa không chỉ sản xuất ra các
cytokin hoặc thực hiện các chức năng hiệu ứng của chúng mà còn chết
tế bào theo chương trình. Trong quá trình này, thụ thể tử vong (Fas)
và phối tử (FasL) của nó đóng một vai trò quan trọng. Do đó, các tế
bào T bình thường biểu hiện Fas nhưng không phải FasL. Khi hoạt hóa,
các tế bào T biểu hiện FasL liên kết với Fas và hoạt hóa quá trình
chết theo chương trình bằng cách kích hoạt caspase-8. Tầm quan trọng
của Fas và FasL được thể hiện rõ bằng quan sát ở những con chuột bị
đột biến ở Fas (đột biến lpr) hoặc FasL (đột biến gld) phát triển
bệnh bạch cầu lympho và tự miễn dịch nghiêm trọng và chết trong vòng
6 tháng trong khi những con chuột bình thường sống tới 2 năm. Những
đột biến tương tự ở các gen chết theo chương trình này ở người dẫn
đến một bệnh bạch cầu lympho gọi là hội chứng phân chia lympho tự
miễn (ALPS).
Vô cảm dòng
Các tế bào T tự phản ứng khi tiếp xúc với các peptid
kháng nguyên trên các tế bào trình diện kháng nguyên (APC) không có
các phân tử đồng kích thích CD80 (B7-1) hoặc CD86 (B7-2) trở thành
vô cảm (không đáp ứng) với kháng nguyên. Ngoài ra, trong khi hoạt
hóa các tế bào T thông qua CD28 kích hoạt sản xuất IL-2, hoạt hóa
CTLA4 dẫn đến ức chế sản xuất IL-2 và vô cảm. Ngoài ra, các tế bào B
khi tiếp xúc với một lượng lớn kháng nguyên hòa tan sẽ làm giảm sIgM
và trở thành vô cảm. Những tế bào này cũng làm tăng biểu lộ các phân
tử Fas trên bề mặt của chúng. Sự tương tác của các tế bào B này với
các tế bào T mang Fas-ligand làm cho chúng chết theo chương trình
Không nhận biết dòng
Các tế bào T phản ứng với tự kháng nguyên không có
trong tuyến ức sẽ trưởng thành và di chuyển đến ngoại vi, nhưng
chúng có thể không bao giờ gặp phải kháng nguyên thích hợp vì nó bị
cô lập trong các mô không thể tiếp cận. Các tế bào như vậy có thể
chết vì thiếu kích thích. Các tế bào B tự phản ứng, thoát khỏi việc
xóa dòng, có thể không tìm thấy kháng nguyên hoặc trợ giúp của tế
bào T đặc hiệu và do đó không được kích hoạt và chết.
Kháng thể kháng idiotyp
Đây là những kháng thể được tạo ra để chống lại những
idiotyp của các kháng thể khác. Kháng thể kháng idiotyp được tạo ra
trong quá trình dung nạp hóa và đã được chứng minh ở động vật dung
thứ. Những kháng thể này có thể ngăn thụ thể tế bào B tương tác với
kháng nguyên.
Các tế bào T điều hòa (Trước đây gọi là các tế bào ức chế)
Gần đây, một quần thể tế bào T khác biệt đã được phát
hiện gọi là tế bào T điều hòa. Các tế bào T điều hòa có nhiều đặc
điểm, nhưng đặc trưng nhất là các tế bào biểu lộ CD4 + và CD25 +. Vì
các tế bào T CD4 bình thường hoạt hóa cũng biểu lộ CD25, nên rất khó
phân biệt các tế bào T điều hòa và tế bào T hoạt hóa. Nghiên cứu mới
nhất cho thấy các tế bào T điều hòa được xác định bằng biểu lộ của
yếu tố phiên mã Foxp3. Biểu lộ của Foxp3 là cần thiết cho sự phát
triển và chức năng tế bào T điều hòa. Các cơ chế chính xác thông qua
đó các tế bào T điều hòa ức chế chức năng tế bào T khác là không rõ
ràng. Một trong những cơ chế là sản xuất các cytokin ức chế miễn
dịch như TGF-và IL-10. Đột biến gen ở Foxp3 ở người dẫn đến sự phát
triển của một rối loạn tự miễn nghiêm trọng và nhanh chóng gây tử
vong được gọi là rối loạn miễn dịch, bệnh Polyendocrinopathy,
Enteropathy, X-link (IPEX). Bệnh này cung cấp bằng chứng nổi bật
nhất cho thấy các tế bào T điều hòa đóng vai trò quan trọng trong
việc ngăn ngừa bệnh tự miễn.
Chấm dứt dung thứ
Thử nghiệm gây ra dung thứ bằng thực nghiệm có thể
được chấm dứt bằng cách không tiếp xúc lâu dài với tologen, bằng các
phương pháp điều trị làm tổn hại nghiêm trọng hệ thống miễn dịch (chiếu
xạ x) hoặc bằng cách mẫn cảm với các kháng nguyên phản ứng chéo.
Những quan sát này có ý nghĩa trong việc khái niệm hóa các bệnh tự
miễn.
|
| |
TỰ MIỄN DỊCH
ĐỊNH NGHĨA
Tự
miễn dịch có thể được định nghĩa là sự cố của các cơ chế đáp ứng về tự
dung thứ mà gây ra đáp ứng miễn dịch chống lại các thành phần của bản
thân. Đáp ứng miễn dịch như vậy có thể không phải lúc nào cũng có hại (ví
dụ: kháng thể chống idiotyp). Tuy nhiên, trong nhiều bệnh tự miễn, người
ta nhận ra rằng các sản phẩm của hệ thống miễn dịch gây ra tổn thương
cho bản thân.
CƠ
CHẾ HIỆU QUẢ TRONG BỆNH TỰ MIỄN
Cả
kháng thể và tế bào T hiệu ứng đều có thể liên quan đến tổn thương trong
các bệnh tự miễn.
PHÂN LOẠI CHUNG
Bệnh
tự miễn thường được phân loại dựa vào cơ quan hoặc mô liên quan bị bệnh.
Những bệnh này có thể thuộc một cơ
quan cụ thể, trong đó đáp ứng miễn dịch hướng vào kháng nguyên (s) liên
quan đến cơ quan đích bị tổn thương hoặc một loại không phải là cơ quan
cụ thể trong đó kháng thể được hướng vào kháng nguyên không liên quan
đến kháng nguyên cơ quan đích (Bảng 2). Kháng nguyên liên quan đến hầu
hết các bệnh tự miễn là rõ ràng từ tên của bệnh (Bảng 2).
XU
HƯỚNG DI TRUYỀN CỦA BỆNH TỰ MIỄN
Các
nghiên cứu trên chuột và quan sát ở người cho thấy xu hướng di truyền
đối với các bệnh tự miễn. Mối liên quan giữa một số loại HLA và các bệnh
tự miễn đã được ghi nhận (HLA: B8, B27, DR2, DR3, DR4, DR5, v.v.).
|
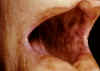 Hình 1
Hình 1
Sự tăng sắc tố của niêm mạc hai bên trong bệnh Addison
© Bristol Biomedical
Archive. Used with permission
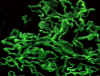 Hình 2
Hình 2
Nhuộm
huỳnh quang miễn dịch của immunoglobulin G (IgG) cho thấy kiểu đường vẽ
trong Hội chứng Goodpasture.
©
Bristol Biomedical Archive. Used with permission
 Hình 3
Hình 3
Da bọng nước - miễn dịch huỳnh quang
©
Bristol Biomedical Archive. Used with permission
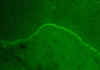 Hình 4
Hình 4
Da bọng nước màng nhầy - miễn dịch huỳnh quang
© Bristol Biomedical Archive.
Used with permission
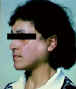 Hình 5
Hình 5
Phì đại tuyến mang tai trong hội chứng Sjogren
©
Bristol Biomedical Archive. Used with permission
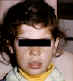
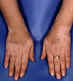 Hình 6
Hình 6
Sự giảm sắc tố ở bệnh bạch biến
©
Bristol Biomedical Archive. Used with permission
|
NGUYÊN NHÂN
BỆNH TỰ MIỄN
Nguyên nhân
chính xác của các bệnh tự miễn chưa
được rõ. Tuy nhiên, các giả thuyết khác nhau đã được đưa ra. Chúng bao gồm kháng
nguyên cô lập, thoát khỏi các dòng tự phản ứng, mất tế bào ức chế, kháng nguyên
phản ứng chéo bao gồm kháng nguyên ngoại sinh (mầm bệnh) và tự kháng nguyên thay
đổi (nhiễm virut và chất hóa học).
Kháng
nguyên cô lập
Các tế
bào của cơ quan lympho có thể không được tiếp xúc với một số tự kháng nguyên
trong quá trình biệt hóa của chúng, bởi vì chúng có thể là kháng nguyên phát
triển muộn hoặc có thể bị giới hạn ở các cơ quan đặc biệt (ví dụ: tinh hoàn,
não, mắt, v.v.). Kháng nguyên được
giải phóng từ các cơ quan này do chấn thương hoặc phẫu thuật có thể dẫn đến
việc kích thích đáp ứng miễn dịch và khởi phát một bệnh tự miễn.
Thoát
khỏi dòng tự phản ứng
Sự chọn
lọc âm ở tuyến ức có thể không đầy đủ chức năng để loại bỏ các tế bào tự
phản ứng. Không phải tất cả các tự kháng nguyên đều hiện diện ở tuyến ức
hoặc các kháng nguyên nào đó có thể không được xử lý và trình diện đúng.
Thiếu
tế bào T điều hòa
Có ít tế bào T
điều hòa trong nhiều bệnh tự miễn.
|
Bảng 2
Phổ
các bệnh tự miễn, các cơ quan đích và các xét nghiệm chẩn đoán |
|
|
Bệnh |
Cơ
quan |
Kháng
thể chống |
Xét
nghiệm chẩn đoán |
|
Đặc hiệu
cơ quan

Không đặc hiệu cơ
quan
|
Viêm tuyến giáp Hashimoto
|
Tuyến giáp |
Thyroglobulin,
peroxidase tuyến giáp (microomal) |
RIA, CF, đông máu
|
|
Phù niêm nguyên phát |
Tuyến giáp |
Thụ thể TSH bào tương
|
Miễn dịch
huỳnh quang (IF) |
|
Bệnh Graves |
Tuyến giáp |
|
Thử nghiệm sinh học, Cạnh tranh đối với thụ thể TSH
|
|
Thiếu máu ác
tính |
Hống cầu |
Yếu tố nội
(IF), Tế bào thành dạ dàyll |
B-12 gắn
vào IF
Miễn dịch
huỳnh quang (IF) |
Bệnh Addison
(Hình
1) |
Thượng
thận |
Tế bào thượng
thận |
Miễn dịch
huỳnh quang (IF) |
|
Mãn kinh khởi phát sớm
|
Buồng trứng |
Tế bào sản
xuất steroid |
Miễn dịch
huỳnh quang (IF) |
|
Vô sinh nam |
Tinh trùng |
Tinh trùng |
Ngưng kết,
Miễn dịch
huỳnh quang (IF) |
|
Đái tháo đường
phụ thuộc insulin
|
Tuyến tụy |
Tế bào bêta
đảo tụy |
|
|
Đái tháo đường
dó kháng Insulin
|
Hệ thống |
Thụ thể
Insulin |
Cạnh tranh thụ thể |
|
Dị ứng |
Hệ thống |
Thụ thể beta-adrenergic
|
Cạnh tranh thụ
thể |
|
Nhược
cơ |
Cơ |
Cơ,
thu thể acetyl cholin
|
Miễn dịch huỳnh quang (IF), Cạnh tranh thụ thể
|
|
Hội chứng Goodpasture
|
Thận, phổi
|
Màng cơ bản
của phổi và thận |
Miễn dịch
huỳnh quang (IF) (linear staining) (Hình
2) |
|
Bệnh mụn nước |
Da |
Phức hợp liên
kết phụ tuộc canxi |
Miễn dịch
huỳnh quang (IF) (Hình
3) |
|
Pemphigoid |
Da |
Màng đáy da
|
Miễn dịch
huỳnh quang (IF) (Hình
4) |
|
Viêm màng bồ
đào |
Thủy tinh thể |
Protein thủy
tinh thể |
|
|
Thiếu máu
huyết tán do AI |
Hồng cầu, tiểu
cầu |
Hồng cầu |
Ngưng
kết thụ động
Coomb trực
tiếp |
|
Giảm tiểu cầu vô căn
|
|
Tiểu cầu |
Miễn dịch
huỳnh quang (IF) |
|
Xơ gan mật tiên phát
|
Gan |
Ty thể |
Miễn dịch
huỳnh quang (IF) |
|
Giảm bạch cầu vô căn
|
Bạch
cầu trung tính |
Bạch cầu trinh
tính |
Miễn dịch
huỳnh quang (IF) |
|
Viêm loét đại
tràng |
Đại tràng |
Lipopolysaccharid đại tràng
|
Miễn dịch
huỳnh quang (IF) |
|
Hội chứng
Sjogren |
Tuyến tiết
(Hình
5)
|
Ống ti thể |
Miễn dịch
huỳnh quang (IF) |
|
Bệnh bạch biến |
Da, Khớp
|
Tế bào hắc tố
(Hình
6) |
Miễn dịch
huỳnh quang (IF) |
|
Viêm khớp dạng
thấp |
Da, thận, khớp,
v.v. |
IgG |
Ngưng kết hạt
latex IgG |
|
Lupus ban đỏ
hệ thống
|
Khớp,
etc. |
DNA, RNA,
nucleoproteins
|
RNA-, Ngưng
kết hạt latex-ADN,
IF (dạng
hạt trong thận) |
|
|
|
|
|
|
Các bệnh
được liệt kê từ cơ quan đặc hiệu nhất (trên cùng) đến ít đặc hiệu nhất (dưới
cùng) |
Kháng
nguyên chéo
Kháng
nguyên ở một số mầm bệnh nhất định có thể có các quyết định kháng nguyên
phản ứng chéo với tự kháng nguyên và đáp ứng miễn dịch chống lại các quyết
định kháng nguyên này có thể dẫn đến tế bào hiệu ứng hoặc kháng thể chống
lại các kháng nguyên của mô. Viêm thận do liên cầu khuẩn và viêm tim, kháng
thể anticardiolipin trong bệnh giang mai và sự liên quan giữa Klebsiella và
viêm cột sống dính khớp là những ví dụ về phản ứng chéo như vậy.
CHẨN ĐOÁN
Chẩn đoán
các bệnh tự miễn dựa trên các triệu chứng và phát hiện các kháng thể (và/hoặc tế
bào T ở thời điểm rất sớm) đáp ứng chống lại các kháng nguyên của các mô và tế
bào liên quan. Các kháng thể chống lại các kháng nguyên liên quan đến tế bào/mô
được phát hiện bằng phương pháp miễn dịch huỳnh quang. Các kháng thể chống lại
các kháng nguyên hòa tan thường được phát hiện bằng ELISA hoặc miễn dịch phóng
xạ miễn dịch (xem bảng trên). Trong một số trường hợp, có thể sử dụng xét nghiệm
sinh học/sinh hóa (ví dụ: bệnh Graves, thiếu máu ác tính).
ĐIỀU TRỊ
Mục tiêu của
điều trị rối loạn tự miễn là giảm triệu chứng và kiểm soát đáp ứng tự miễn, đồng
thời duy trì khả năng chống nhiễm trùng của cơ thể. Phương pháp điều trị rất
khác nhau và phụ thuộc vào bệnh và triệu chứng cụ thể: Thuốc chống viêm
(corticosteroid) và thuốc ức chế miễn dịch (như cyclophosphamid, azathioprin,
cyclosporin) là phương pháp điều trị bệnh tự miễn hiện nay. Nghiên cứu mở rộng
đang được thực hiện để phát triển các phương pháp điều trị cải tiến bao gồm:
liệu pháp kháng TNF anpha chống viêm khớp, đưa kháng nguyên bằng đường uống để
kích hoạt dung nạp, kháng thể chống idiotyp, peptid kháng nguyên, kháng thể
kháng thụ thể IL2, kháng thể kháng CD4, kháng thế kháng TCR…
MÔ HÌNH
BỆNH TỰ MIỄN
Có một số mô
hình động vật thí nghiệm và tự nhiên để nghiên cứu các bệnh tự miễn. Các mô hình
thí nghiệm bao gồm viêm não dị ứng tự miễn thực nghiệm, viêm tuyến giáp thực
nghiệm, viêm khớp do thuốc bổ trợ.
Các mô hình
tự nhiên của các bệnh tự miễn bao gồm thiếu máu tan máu ở chuột New Zealand,
bệnh lupus ban đỏ hệ thống ở New Zealand /New Zealand (BW), chuột BXSB và MRL và
bệnh tiểu đường ở chuột béo phì.
|

 Hình 1
Hình 1 






