![]()

Dr Richard Hunt
VIROLOGÍA – CAPÍTULO SIETE PARTE NUEVE
EL VIRUS DE LA INMUNODEFICIENCIA HUMANA Y EL SIDA
El Genoma del VIHTraducido por :
Sarah M. Castillo - Jorge, Clinica Corominas
Santiago, Rep. Dominicana
VIDEOCONFERENCIA
EN INGLÉS
ENLACES A OTRAS SECCIONES DE VIH Y SIDA AL FINAL DE ESTAPAGINA
HAGA CLICK EN LOS RECUADROS GRISES PARA VENTANAS RAPIDAS CON MÁS INFORMACIÓN
HAGA CLICK EN LOS RECUADROS AMARILLOS PARA SER REDIRECCIONADO A OTROS CAPÍTULOS

Figura 24A El genoma del VIH-1

Figura 24B La estructura de la gp160.
A. El dominio linear de la estructura de la gp160 se muestra arriba. La
Gp160 es segmentada en gp120 (la proteína de superficie) y en gp41 (la
proteína transmembrana de fusión).
B. Un trímero de gp120/gp41 se asocial a la membrana viral.
C. La Gp120 tiene un número de dominios hipervariables (V1-V5). Las barras
rojas muestran puentes bisulfuro
Dado que el VIH tiene un ciclo de vida más complejo que los retrovirus más simples como el Virus del Sarcoma Rous y parece que el VIH puede controlar su replicación de una manera más compleja, se podría esperar más información genética, pero este no es el caso. El genoma del VIH es de 9749 nucleótidos – casi del mismo tamaño que otros retrovirus, por ejemplo el virus del sarcoma Rous (RSV).
El genoma del VIH es más complejo que el RSV, no obstante, puesto que tiene marcos de lectura abiertos adicionales que claramente codifican pequeñas proteínas (figura 24a). Los anticuerpos contra estas proteínas se encuentran en personas VIH-infectadas. Algunas de estas son proteínas de control de síntesis proteica.
El genoma del VIH tiene nueve marcos de lectura abiertos (conllevando a nueve productos primario de traducción) pero se sintetizan 15 proteínas como resultado de la segmentación de tres productos primarios.
El gen GAG y los
genes GAG y POL juntos se traducen a grandes poli proteínas que son luego
segmentadas por una proteasa codificada por el virus que es parte de la poli
proteína POL.
La poli proteína GAG e segmentada en cuatro proteínas que se hayan en el virus
maduro: MA (matriz), CA (cápside), NC (nucleocápside), p6
| Más sobre la CA | Más sobre la NC | Más sobre la P6 |
La poli proteína POL es segmentada en: PR (proteasa), RT (transcriptasa inversa), IN (integrasa)
| Más sobre la PR | Más sobre la RT | Más sobre la IN |
El gen ENV se traduce en una poli proteína (Gp160) que luego es segmentada por una proteasa de la célula huésped (llamada furina) que se encuentra en el Cuerpo de Golgi. No es segmentada por una proteasa codificada por el virus. La Gp160 es segmentada a: SU (Gp120) y TM (Gp41). Esta última retiene la parte transmembrana de la Gp160 mientras que la Gp120 permanece unida a la Gp41 mediante enlaces no covalentes.
Además de las nueve proteínas derivadas de GAG, POL y ENV, hay otras seis proteínas sintetizadas por el VIH. Tres de éstas son incorporadas al virus (Vif, Vpr y Nef), mientras que otras no se encuentran en el virus maduro: Tat y Rev son proteína reguladoras y Vpu indirectamente ayuda en el ensamblaje. Los genes que codifican estas proteínas se conocen por sus nombres de tres letras derivados así:
TAT: Trans-Activadora de la Transcripción
REV: Reguladora de la expresión de las proteínas del Virión
NEF: Factor Regulador Negativo
VIF: Factor de Infectividad del Virión
VPU: Proteína Viral U
VPR: Viral Proteína R
Estaos genes codifican proteínas pequeñas; la TAT por ejemplo consiste de 88 amino ácidos. Estos se solapan con los genes estructurales (especialmente ENV) pero están en diferentes marcos de lectura. Del diagrama de arriba de la organización del genoma del VIH (figura 24), se puede ver que algunas se codifican en dos exones (a diferencia de los genes estructurales) y por tanto sus ARNm puede ser derivados mediante empalmes alternativos de los ARNm de los genes estructurales. Esto es un tanto importante para la forma que en los niveles de éstas son controlados. Los mutantes en los genes TAT y REV muestran que ambas proteínas son necesarias para la producción del virus.
TAT
El producto del gen TAT se une a una secuencia en todos los genes del VIH y estimula positivamente la transcripción. Por tanto es un regulador positivo de la síntesis proteica, incluyendo su propia síntesis.
REV
REV se une a un elemento sólo en el ARNm de proteínas estructurales (GAG/POL/ENV) y regula el radio de GAG/POL/ENV a proteínas no estructurales controladoras de la síntesis proteica (TAT/REV). Cuando los niveles de REV son altos, la síntesis de proteínas estructurales aumenta y la síntesis de proteínas controladoras disminuye. Por tanto, la REV inhibe su propia producción y la de la TAT.
El resultado normal es la homeostasis, baja o ninguna producción viral y latencia en las células CD4 de reposo.
Hay un problema inherente en el estilo de vida del VIH. Este utiliza ARN genómico como su ARN mensajero. Este ARN no está empalmado y el núcleo posee un mecanismo que impide a los ARNm no empalmados salir del mismo y ser traducidos. Es trabajo del Rev el superar este problema.

 Figura
25
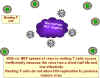
Efectos de la NEF en el CD4
Figura
25
Efectos de la NEF en el CD4
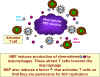 Figura 26 La NEF induce a las citocinas que atraen a las células T a un
macrófago infectado
Figura 26 La NEF induce a las citocinas que atraen a las células T a un
macrófago infectado
NEF
La proteína Nef es sintetizada en etapas tempranas de la infección. A pesar de su pequeño tamaño la NEF tiene varias funciones.
a) La homeostasis implica problemas para el pro virus parasítico:
i) Sobre-infección por otras partículas del VIH que se unen a los antígenos CD4 de superficie y pueden eliminar la célula.
ii) Probablemente más importante, el virus unido mediante el antígeno CD4 en la superficie celular o la Gp120 unida al antígeno CD4 puede dar como consecuencia que la célula sea sujeta a un ataque inmune y sea destruida.
La traducción del gen NEF como resultado del primer virus infectante causa la integración del antígeno CD4 de la superficie celular y su destrucción en lisosomas (figura 25). Por tanto ¡ningún VIH ni ninguna gp120 pueden unirse a la superficie de una célula infectada!
b) Por un mecanismo diferente de su regulación a la baja del antígeno CD4, la proteína NEF reduce la expresión de las moléculas CMH de clase I en la superficie. Esto altera la presentación antigénica de la célula infectada y se supone que protege a la célula infectada de un ataque por células T citotóxicas.
c) El nombre, NEF, proviene de factor negativo. Originalmente, se creía que los viriones que carecían de la NEF crecían mejor que las cepas silvestres. Ahora el consenso general es justo lo opuesto, que es ese virus producido en la presencia de NEF es un poco más infeccioso que el virus que se produce en su ausencia.
d) Se ha encontrado que la NEF es importante para la replicación del VIH in vivo pero esto parece darse en mucho menor medida en los cultivos in vitro. La razón de esto aún no está esclarecida. Recientemente, esta cuestión parecía estar resuelta. La respuesta se halló en los macrófagos los cuales son cambiados de dos formas cuando se infectan por in VIH que expresa el NEF (recuerde que los macrófagos son células que entran el VIH al cuerpo y las cepas iniciales del VIH en un paciente infectado son macrófago – trópicas).
Los macrófagos VIH – infectados secretan MIP-1alfa y MIP-1beta. Estas son dos quimiocinas que se unen a los co-receptores para la infección del VIH en los macrófagos pero estas quimiocinas tienen otra función.
Probaron que las células t CD4+ migran (bajo efectos de quimiotaxis) hacia los macrófagos infectados (figura 26). Esto es importante in vivo puesto que, inicialmente, las células VIH – infectadas no son muy numerosas y las células T no infectadas pueden no encontrarse en la vecindad de las células infectadas. Más aún, el VIH no tiene una vida media larga en la circulación antes de hacerse no-infeccioso. La migración de células no infectadas hacia las células infectadas aumenta la probabilidad de que las células T se encuentren con macrófagos infectados antes de salir del sistema retículoendotelial. Esto explica porqué la NEF parece no tener mucha consecuencia en los cultivos células cuando ya las células están cerca una de otra. Los macrófagos infectados hacen otra cosa. Sintetizan un factor que todavía no ha sido identificado el cual activa a las células T en reposo que han sido atraídas hacia ellos permitiéndoles ser productivamente infectadas y descamar nuevas partículas del virus (Recuerde, que los lentivirus, a diferencia de otros retrovirus pueden infectar células que no están en división. Normalmente, los retrovirus solo pueden entrar al núcleo e integrarse durante la mitosis cuando la membrana nuclear es segmentada; sin embargo, las proteínas de los lentivirus como el VIH tiene moléculas de señalización nuclear que permiten a la nucleocápside encontrar el poro nuclear. Así, el virus puede integrarse a los cromosomas de la célula huésped en donde pueden codificar más proteínas y ARN virales. El VIH, contrario a otros lentivirus, no transcribe su genoma a ARN en células T en reposo dado que la activación del promotor en las secuencias LTR necesita de factores de transcripción que únicamente se sintetizan cuando la célula en reposo se activa). Estos hallazgos explicar porqué los macrófagos son vitales para la diseminación del VIH.
Nota: In vivo, el VIH puede infectar células T en reposo pero no puede replicarse en ellas. Aunque la NEF puede activar la célula, esto no puede hacerse en una célula T en reposo. Las observaciones antes mencionadas resuelven este acertijo. Los macrófagos son infectados por el VIH y sintetizan la NEF sin ningún proceso de activación. Como resultado sintetizan factores que activan a las células T en reposo que ¡ya podrán soportar una infección productiva!
VPU
Luego de la activación de la célula T, el virus se encuentra con otro problema: el antígeno CD4 y la Gp120 se sintetizan en el retículo endoplásmico en la misma célula. Es probable que se unan entre sí antes de alcanzar la membrana plasmática y dichos complejos son usualmente susceptibles de degradación celular. Para detener las cosas, otra de las pequeñas proteínas del VIH (VPU) promueve la proteolisis del antígeno CD4 de la célula huésped ¡mientras se sintetiza!
La VPU también aumenta la liberación de partículas virales desde la célula huésped. No está claro como lleva a cabo esta función pero la VPU forma un canal iónico en la membrana plasmática de la célula huésped y puede alterar la composición iónica del citoplasma. También se une a una proteína celular (proteína fijadora de VPU o UBP) y la sobre-expresión de esta proteína disminuye el efecto potenciador de la VPU en la liberación viral. La UBP puede ser un factor negativo para el ensamblaje que debe d ser desplazado de las proteínas GAG antes de que un virus pueda ensamblarse en la superficie celular.
La VPU forma un poro de transporte iónico en la membrana superficial que conduce pequeños iones como el Na y el K. La habilidad de la VPU de formar canales y su habilidad de potenciar la liberación viral parecen estar correlacionadas.
De su habilidad para estimular la liberación viral y de segmentar el antígeno CD4 (que son funciones separadas de diferentes partes de la molécula de VPU), parece que la VPU potencia la patogenicidad del virus al aumentar el número de partículas de VIH por célula.
VIF
La proteína Vif
(factor de infectividad viral), que es esencial para la infección in vivo,
puede ser muy importante en la supresión de la resistencia a la infección del
VIH por parte del huésped. La VIF es necesaria durante las fases tardías de la
producción viral y parece funcionar suprimiendo las actividades anti-virales
innatas en las células T y en los macrófagos, las principales células infectadas
en los humanos. Sin la VIH, el VIH no es infeccioso en células T humanas
primarias.
¿Qué es lo que hace a las células T susceptibles de ser activadas contra el VIH
cuando la VIH está ausente? Se cree que la VIH es necesaria para la producción
de partículas víricas infecciosas puesto que inhiben la cascada antiviral en las
células que implica una enzima denominada APOBEC3G (originalmente descubierta
como enzima editora de la apolipolproteína B del ARN mensajero). Esta enzima es
una citidina deaminasa que también ataca al ADN de cadena sencilla. Parece que
la VIH previene la edición del ADN viral de cadena sencilla que es el producto
inicial de la transcriptasa inversa. Tal edición es mucho más pronunciada cuando
el virus infeccioso tiene una deleción del VIF. Entonces, el VIH previene muchas
mutaciones que implicarían cambios en las proteínas estructurales, enzimas y
proteínas reguladoras que de otro modo conllevaría a la pérdida de la
infectividad viral.
VPR
La VPR influencia la patogénesis del VIH y es esencial para la infección de los macrófagos, y, en menor medida, de otras células. También activa la transcripción del VIH promovida por LTR. Causa un arresto en la división de la célula huésped en el estadio G2 del ciclo celular y apoptosis de la célula infectada. Actúa como una proteína transbordadora entre el citoplasma y el núcleo (para el complejo de pre-integración a través de los poros nucleares). La VPR se encuentra en el suero de los pacientes infectados con el VIH.
FUENTES EN LA RED
OTRAS SECCIONES SOBRE EL VIH
PARTE I VIRUS DE LA INMUNODEFICIENCIA HUMANA Y EL SIDA
PARTE II VIH Y SIDA, LA ENFERMEDAD
PARTE III CURSO CLÍNICO DE LA ENFERMEDAD
PARTE IV PROGRESIÓN Y COFACTORES
PARTE VI SUBTIPOS Y CO-RECEPTORES
PARTE VII COMPONENTES Y CICLO DE VIDA DEL VIH
PARTE X PERDIDA DE CÉLULAS CD4
PARTE XI OTRAS CÉLULAS INFECTADAS POR EL VIH Y POLIMORFISMOS POBLACIONALES
APÉNDICE II ¿ES EL VIH CAUSA DE SIDA?
APÉNDICE III QUIMIOTERAPIA ANTI-VIH